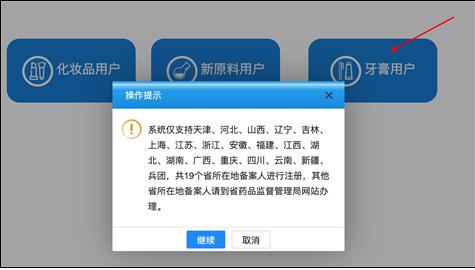
[더케이뷰티사이언스] 중국 시장에서 치약 제품을 판매하려면 오는 12월 1일부터 중국 ‘치약등록정보서비스 플랫폼(牙膏备案信息服务平台)’을 통해 제품 정보를 의무적으로 등록해야 한다.
중국 국가약품감독관리국(NMPA)은 ‘치약 감독관리조치’ 규범에 따라 치약 규제 요구사항과 현재 시판중인 치약의 간소화 등록 요건에 관한 사항을 지난 9월 25일 발표했다. 이는 올 3월 23일 중국 국가시장관리감독총국(SAMR)이 발표한 ‘치약감독관리방법’에 대한 구체적인 제품 등록에 관한 고시다.
이번 고시의 주요 내용은 중국으로 수출되는 치약 제품들은 올해 12월 1일부터 제품 출시 이전에 ‘치약 정보서비스 플랫폼’을 통해 등록을 필수로 진행해야 한다. 또한 제품 등록 시 제품 효능에 대한 근거자료 개요도 함께 제출이 요구된다. 다만 ‘청결’ 효능만 클레임하는 제품은 효능 근거자료 개요 제출이 면제된다. 이 플랫폼은 지난 9월 22일 개통됐다.
또, 12세 이하 어린이용 치약도 규정됐다. 어린이용 치약은 청결, 충치 예방 효능만을 클레임할 수 있다. 이 외에도 어린이용 치약 로고 사용 방법, 경고 문구 표기 항목에 대해 설명했다.
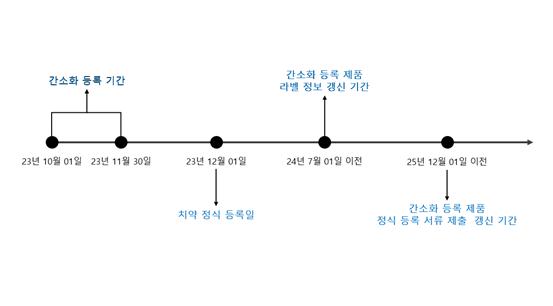
이번 고시에 따라 기존에 현지에서 판매 중인 치약 제품들은 오는 2023년 10월 1일부터 11월 30일까지 간소화 등록이 가능하다. 이들 제품은 일정 기간 사용되면서 안전성이 입증되어 제출 정보 요건을 단순화했다. 간소화 등록 시 제출되는 정보는 등록인 기본 정보(회사명, 주소, 연락처 등), 제품 기본 정보(제품명, 처방, 라벨 정보), 제품의 안전 사용 이력 증빙서류(제품 생산 기록서, 판매 영수증, 시험보고서 등) 등이다. 하지만 간소화 등록 제품들도 오는 2025년 12월 1일 이전까지 모든 등록 서류를 제출해야 한다. 특히 간소화 등록을 진행할 경우 제품의 최초 출시일, 라벨 정보, 효능 정보에 따른 시간표에 따라 별로 플랫폼에 해당 정보를 갱신 하도록 요구하고 있어 기업들은 제품 별로 제출 정보 갱신 기간을 사전에 숙지하고 대비해야 한다.
리이치24시코리아 최우영 선임연구원은 “중국에서 시판중인 치약 제품은 올 10월부터 두 달 동안만 간소화 등록이 가능하고, 오는 12월 1일부터 신규 등록을 한 뒤 제품 수출이 가능하기 때문에 발빠르게 움직여야 한다”고 설명했다.