‘2023년 주요 업무계획’ 발표
[더케이뷰티사이언스] 식품의약품안전처(처장 오유경)는 1월 9일 ‘안전혁신으로 국민의 일상을 든든하게, 규제혁신으로 식의약 산업을 단단하게’를 핵심 목표로 8가지 주요 정책과제를 담은 ‘2023년 주요 업무계획’을 발표했다.
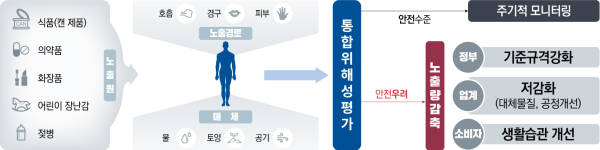
이 가운데 사람 중심의 통합위해성평가를 본격적으로 시행한다. 다양한 경로로 노출되는 유해물질을 제품이 아닌 사람 중심으로 총량 관리하기 위한 ‘제1차 위해성평가 기본계획’(2023~2027년)을 시행한다. 제1차 위해성평가 기본계획은 유해물질 52종 선정·평가, 평가 정보 수집 및 기술 개발, 유해물질 저감기술 개발, 국민 체감 위해소통 및 관계부처 협력 강화 등이 담겨 있다.
올해에는 국내외 이슈, 위해성 보고사례 등을 고려해 프탈레이트(환경호르몬) 등 8종을 우선 평가하고, 결과를 반영해 관리 필요시 기준·규격 강화, 공정개선 및 대체물질 사용으로 노출량 저감화를 유도한다. 또 평가 결과를 공개해 노출량·노출원, 위해정도를 알리고 ‘소비자 평가요청제’를 통해 소비자 우려를 꼼꼼하게 검증한다.
또 마이크로바이옴, 엑소좀 등 신개념‧신기술 의약품의 정의, 분류기준을 마련하고, 제품 특성을 고려한 허가심사 자료요건 및 시설기준을 제시한다.
규제지원 가교를 통해 혁신제품 출시를 가속화한다. 이를 위해 제품별 담당자(PM)를 통한 개발전략 맞춤상담(With-U)부터 혁신제품 신속심사 프로그램(GIFT) 운영까지 전주기 제품화 집중지원을 제공한다.
국가 R&D의 기획 단계부터 규제대상 여부, 제품분류, 평가기술 필요성을 동시에 검토하는 기술-규제 정합성 검토대상을 확대(4→6개)한다.
또 규제과학대학원(8개 분야)에서 석·박사급 전문인재를 양성(2023~2027년, 600명)하고 산업현장의 규제업무 전문가를 양성(2023~2027년, 2만4120명)한다.

이와함께 혁신제품에 대한 안전평가 연구 및 제품화 지원, 전문인력 양성 등 전반에 관해 규율을 담아 체계적인 규제서비스를 위한 식의약규제과학혁신법 제정을 추진하고, 한국규제과학센터의 기능도 확대*해 규제과학 허브 역할을 정립한다.
글로벌 협력 네트워크 강화로 민간 수출애로를 해소한다. 가령 아·태 식품 규제기관장 협의체(APFRAS) 신설을 주도하고, 국제 규제협의체 활동 강화와 주요국 규제기관과 협력채널을 활성화할 계획이다.