황재성 교수(경희대학교 생명과학대학 유전공학과)
서론
그 동안 미백 화장품 개발을 위한 다양한 소재 개발이 진행되어 왔다. 논문 검색을 해보면 최근 몇 년간은 피부 미백 소재와 관련된 논문이 대한민국에서 가장 많이 발표되며, 이러한 현상이 매우 놀랍기도 하고, 많은 연구자들이 이 분야에 관심이 매우 높다고 여겨진다. 발표되는 다양한 연구 논문을 통해 우리는 새로운 지식과 소중한 정보를 얻을 수 있다. 하지만 대다수의 우수한 연구들도 단지 논문으로 끝나며, 실용화되어 제품에 적용되는 경우는 소수에 그치는 아쉬움도 함께한다. 그 동안 보고된 많은 합성 화합물, 천연물 그리고 천연물 유래의 미백 성분들에 대한 많은 리뷰 논문들이 있으며 (1, 2) 이러한 리뷰 논문을 통해 그 동안 개발되거나 보고된 정보를 어렵지 않게 얻을 수 있다. 따라서 본 리뷰에서는 기존의 보고들에 대한 정리 분석 보다는 본 필자가 그 동안 연구하며 얻은 정보와 결과를 중심으로 실용화되었거나, 이와 근접한 미백 소재 개발의 가능성과 한계 그리고 미래를 전망해 보고자 한다.
본론
2.1. 3, 4, 5-Trimethoxycinnamate Thymol Ester(TCTE, Melasolv®)
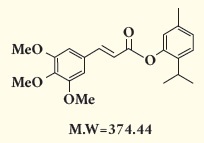
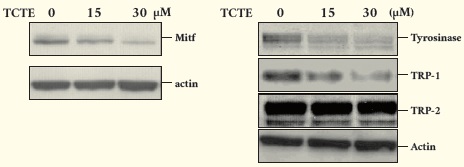
본 소재는 몰식자산을 기본 구조로 합성한 물질로 다양한 유도체들을 합성하고 random screening을 통해 선택된 소재이다 (3, 그림1). 주로 mouse immortalized melanocyte cell line인 melan-a 세포를 이용하여 멜라닌 합성 저해 효능을 주타깃으로 선정되었다. 본 필자 등에 의한 작용기전 연구결과 melan-a 세포에서 멜라닌 형성과 생존에 주요한 전사인자인 Microphthalmia-associated transcription factor (MITF)의 분해를 촉진하는 것으로 나타났다. 따라서 MITF가 관장하는 tyrosinase 및 tyrosinase related protein 1 (TRP-1)의 발현을 저해하여 멜라닌 생성을 억제하는 것으로 보고 되었다 (4, 그림2). 본 소재는 안정도가 우수하고, 세포의 독성이 낮아 2001년 개발된 이후 오랜 기간 동안 다양한 제품에 기능성 미백 소재로 사용되고 있으나, 인체 적용 시 효능 및 피부 흡수 등에 대한 연구가 부족하며, 이에 대한 연구가 뒷받침 된다면 더욱 좋은 소재로 자리잡을 것으로 기대된다.
2.2. IL-6 inducer (Lepidium apetalum extract)
피부에 자외선 등 자극이 전달되면 멜라닌 합성을 촉진시키는 다양한 인자, 즉 prostaglandin E2, α-MSH, adrenocorticotropin-melanocyte-stimulating hormone
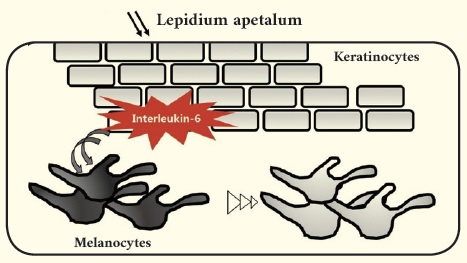
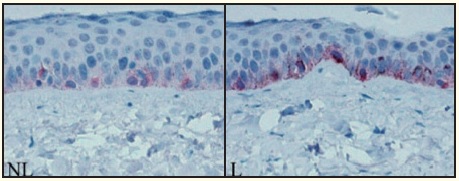
(ACTH), endothelin-1 및 Nitric oxide(NO) 등이 각질형성 세포에서 분비된다. 한편, 일정시간이 지난 후에는 과다한 멜라닌 생성을 막고 균형을 이루기 위해 멜라닌 생성을 억제하는 인자, 즉 interleukinIL-1α, IL-6, tumor necrosis factor(TNF-α) 및 transforming growth factor(TGF-β) 등이 분비된다. 이러한 점에 착안하여 각질형성세포에서 IL-6의 분비를 촉진하는 소재를 개발하였다 (5). 본 소재는 멜라닌 형성세포에 직접 처리하였을 때 멜라닌 생성을 억제하지는 못하나, 각질세포에 처리하고 그 배양액을 멜라닌 형성세포에 처리하면 멜라닌 생성을 억제하였고 (그림 3), 이는 각질세포에서 분비되는 IL-6에 의한 효과였다 (그림 4).
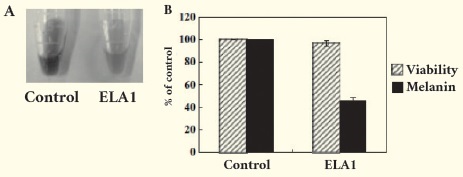
즉, 정력자 추출물Lepidium apetalum extract을 피부에 적용하면, 각질형성세포에서 IL-6의 분비를 촉진시키고, 촉진된 IL-6는 멜라닌세포에서 멜라닌의 합성을 저해하는 것으로 나타났다 (그림 4). 본 소재는 기존의 미백 소재와는 달리, 표피 기저층에 있는 멜라닌형성세포에 전달되지 않아도 표피에서 작용하기 때문에 효과를 잘 발현할 수 있는 큰 장점이 있다. 한편, 주요한 효능성분에 대한 분석이 더 되지 못한 부분이 아쉬움으로 남지만, 각질 형성 세포에 작용하는 미백소재의 가능성이 매우 유효하다는 것이 주요한 시사점으로 생각된다.
2.3. c-Kit inhibitor
일본의 한 회사가 자외선에 의한 색소침착과정에서 Stem Cell Factor(SCF)와 이의
receptor인 c-kit이 중요한 역할을 한다는 연구결과를 발표했다 (6). 이후 본 필자 등은 기미 부위의 피부에서 stem cell factor(SCF)와 그 receptor인 c-kit이 과 발현 된다는 사실을 알게 되었다 (7). 한편 2000년대 초반에 최초로 개발된 표적 항암제인 GLEEVEC®(imatinib mesylate)은 c-kit과 같은 tyrosine kinase family인 Abelson proto-oncogene(able)을 타깃으로 하며, 당시 참석한 한 학회에서 본인은 GLEEVEC®을 처방하는 의사와 대화도중 투여 받은 환자 중 색소가 감소되는 현상이 종종 발견된다는 의견을 들었다. 따라서 아마도 이는 본 약물이 c-kit에 작용하였을 가능성이 있다고 판단되었고, 이를 이용하면 새로운 미백소재를 개발할 수 있을 것으로 판단하였다.
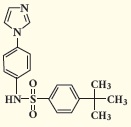
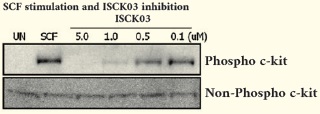
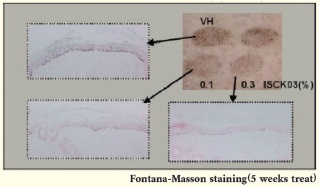
c-kit을 억제하는 소재를 찾기 위해 다양한 화합물을 검색하여 [4-t-Butylphenyl]-N-(4-imidazol-1-yl phenyl) sulfonamide (ISCK03)가 최종후보로 선택되었다 (그림 6), 본 소재는 c-kit의 활성을 억제하고, 피부 색소 형성 및 hair의 색소 형성을 가역적으로 억제하는 우수한 효능을 나타냈다 (8, 그림 7, 그림 8). 하지만, 미백 기능성 인증을 받지 못하여 제품으로 상용화 되지 못하였으나 추가적인 연구를 통해 우수한 소재로 개발될 가능성이 있다고 판단되는 후보이다.
2.4. α-Glucosidase 저해제
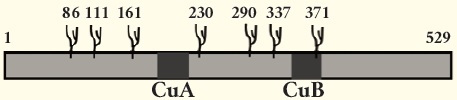
Tyrosinase는 7곳에서 glycosylation이 일어나는 type I glycoprotein으로 알려져 있다(9, 그림 9). 본 필자 등은 glycosylation과정 중에 관여하는 α-glucosidase의 저해제를 사용하여 멜라노마 세포에서 멜라닌 생성을 강력히 저해함을 보고한 바 있다 (10).
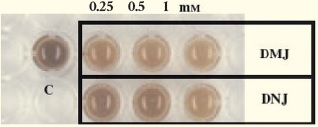
본 연구에 의하면, α-glucosidase 저해제인 deoxynojirimycinDNJ 뿐 아니라, α-1,2-
mannosidase의 저해제인 deoxymannojirimycinDNJ이 tyrosinase의 glycosylation을
억제하며 이에 따라 효소가 불안정해지고 멜라닌 생성이 저해되는 효과가 나타났다 (그림 10).
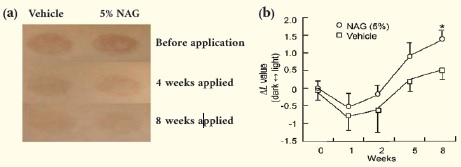
또한, 본 필자 등은 역시 α-glucosidase의 저해제인 N-acetylglucosamineNAG을 5% 농도로 도포하였을 때 사람 피부에서 자외선에 의한 색소침착을 개선시켜 줄 수 있다는 것을 보고하였다 (11, 그림 11). 따라서 α-glucosidase 혹은 glycosylation 저해제는 미백 소재로서 가능성이 매우 높다고 보여진다. 하지만, 본인의 경험으로 유추해 보면 in vitro 결과와 in vivo 결과가 상관성이 낮다는 것과 비교적 고농도를 사용해야 효과가 있다는 것, 그리고 tyrosinase에 특이적으로 작용하는 것이 어렵다는 것이 한계점으로 생각된다.
2.5. Melanosome transport 저해제
본 필자 등은 기존 소재 보다 더욱 안전하면서도 효과 있는 미백 소재를 찾기 위해, 멜라닌 생성을 억제하는 기전에서 벗어나 멜라노좀의 이동을 억제하는 소재를 찾고 이의 가능성을 확인하고자 하였다. 멜라닌 형성 세포 내에서 멜라니 좀의 이동은 actindependent motor protein인 MyosinVa 와 Rab27a 그리고 MelanophilinMlph에 의해 매개된다 (12). Tabebuia avellanedae에서 발견된 2-methyl-naphtho[1,2,3-de] quinolin-8-one (MNQO, 그림 12)은 이러한 세가지 단백질의 발현을 모두 억제하며, 멜라노좀의 이동을 강력히 저해하는 것으로 나타났다 (그림 13).
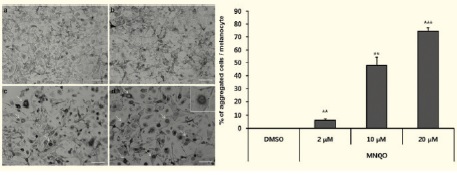
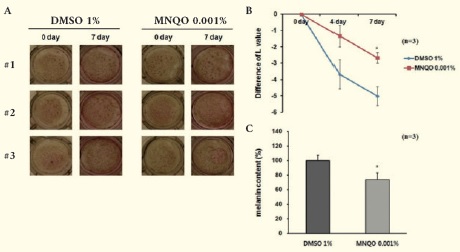
또한, 이러한 저해는 궁극적으로 재조합된 인공 피부에서 멜라닌 생성을 억제하고, 피부색소 침착을 감소시키는 것으로 나타났다 (그림 14). 본 결과를 통해 멜라노좀 이동을 저해하는 것이 피부 색소 침착을 개선시킬 수 있는 좋은 타깃이 될 수 있을 것으로 판단된다. 하지만 궁극적으로는 멜라닌 형성세포에만 특이한 Mlph만을 조절한다면 더욱 안전하고 효과적인 미백 소재가 될 수 있을 것으로 판단되며, 이런 소재를 찾기 위한 방법개발과 기전에 대한 연구를 진행하고 있다.
결론
이상의 결과에서 미백 소재를 찾기 위한 몇 가지의 접근 방법과 발표된 연구 결과 및 제품화 현황 등에 대한 경험을 소개하였다. 본 지면에는 소개하지 않았으나, 기존에 잘 알려져 있고 또한 널리 사용되는 미백 소재를 복합하여 효과를 극대화 하기 위한 in vitro 및 in vivo 연구를 통해 좀 더 우수한 제품을 개발할 수 있는 가능성을 확인하였다. 필자는 본 보고에 포함되는 소재들이나 혹은 향후 개발되는 소재들의 특성을 이용한 복합처방을 개발한다면 더욱 안전하고 우수한 제품 개발이 가능하다는 것을 강조하고 싶다. 하지만, 이 경우 각 개별 소재의 작용 기전, 사용 농도 및 실험 디자인이 매우 중요하며 그렇지 않은 경우 오히려 반대의 결과도 얻어 질 수 있다. 서론에서도 밝혔듯이 현재 국내의 연구자들에 의해 진행되고 있는 우수하고 독창적인 연구들을 통해 혁신적인 소재 개발과 이를 이용한 안전하고 효능 있는 제품이 개발되어 K-뷰티가 더욱 공고해지기를 기대하며 부족한 글을 마무리하고자 한다.
참고 문헌
1. Céline Couteau and Laurence Coiffard. Overview of Skin Whitening Agents: Drugs and Cosmetic Products. Cosmetics. 2016; 3, 27; doi:10.3390/cosmetics3030027,
2. Smit N, Vicanova J, Pavel S The hunt for natural skin whitening agents. Int J Mol Sci. 2009 ; 10(12), 5326-49. doi: 10.3390/ijms10125326.
3. Kang HH, Rho HS, Hwang JS, Oh SG. Depigmenting activity and low cytotoxicity of alkoxy benzoates or alkoxy cinnamte in cultured melanocytes. Chem Pharm Bull (Tokyo). 2003; 51(9), 1085-1088.
4. Hwang, Jae-Sung; Hyunjung Shin; Noh, Ho-Sick; Park, Hyunjung; Ahn, Soo-mi; Park, Dong-Soon; Kim, Duck-Hee; Lee, Byeong-Gon; Ihseop Chang. The inhibitory effects of 3,4,5-Trimethoxy cinnamate thymol ester (TCTE, Melasolv) on Melanogenesis. Journal of the Society of Cosmetic Scientists of Korea. 2002; 28(1),135-149
5. Choi H, Ahn S, Lee BG, Chang I, Hwang JS. Inhibition of skin pigmentation by an extract of Lepidium apetalum and its possible implication in IL-6 mediated signaling. Pigment Cell Res. 2005; 18(6), 439-46.
6. Hachiya A, Kobayashi A, Ohuchi A, Takema Y, Imokawa G. The paracrine role of stem cell factor/c-kit signaling in the activation of human melanocytes in ultraviolet-B-induced pigmentation J Invest Dermatol. 2001; 116(4), 578-86.
7. Kang HY, Hwang JS, Lee JY, Ahn JH, Kim JY, Lee ES, Kang WH. The dermal stem cell factor and c-kit are overexpressed in melasma. British Journal of Dermatology. 2006; 154, 1094–1099.
8. Na YJ, Baek HS, Ahn SM, Shin HJ, Chang IS, Hwang JS. [4-t-butylphenyl]-N-(4-imidazol-1-yl phenyl)sulfonamide (ISCK03) inhibits SCF/c-kit signaling in 501mel human melanoma cells and abolishes melanin production in mice and brownish guinea pigs. Biochem Pharmacol. 2007; 74(5), 780-786.
9. Ujvari A, Aron R, Eisenhaure T. Translation rate of human tyrosinase determines its N-linked glycosylation level. J Biol Chem 2001; 276, 5924–5931.
10. Choi H, Ahn S, Chang H, Cho NS, Joo K, Lee BG, Chang I, Hwang JS. Influence of N-glycan processing disruption on tyrosinase and melanin synthesis in HM3KO melanoma cells. Exp Dermatol. 2007; 16(2), 110-117.
11. Hwang JS, Lee HY, Lim TY, Kim MY, Yoon TJ. Disruption of tyrosinase glycosylation by N-acetylglucosamine and its depigmenting effects in guinea pig skin and in human skin. J Dermatol Sci. 2011;63(3), 199-201.
12. Park JI, Lee HY, Lee JE, Myung CH, Hwang JS. Inhibitory effect of 2-methyl-naphtho[1,2,3-de]quinolin-8-one on melanosome transport and skin pigmentation. Sci Rep. 2016 :29189. doi: 10.1038/srep29189.