박병철 교수(단국대학교 병원 피부과, 단국대학교 의과대학 기초 및 임상 모발연구소)
김순례 박사(단국대학교 의과대학 기초 및 임상 모발연구소, 단국대학교 한국베커만 광 의료기기 연구센터)
서론
일반인들은 통상적으로 머리 빠지는 개수가 증가하거나, 두피 모발의 숱이 감소하면 탈모라고 생각을 한다. 사실 탈모는 질환을 뜻하기 보다는 하나의 증상을 말하는 것으로 탈모라는 증상을 가지면서 다양한 탈모 질환이 발생할 수 있다.[1] 이 글에서는 탈모의 다양한 증상과 원인 그리고 치료제 특히 탈모 완화를 위한 기능성 화장품의 개발을 위한 세포 및 임상 연구 접근법에 대해 다루고자 한다.
본론
Ⅰ 탈모의 종류
탈모는 앞서 하나의 증상이라고 얘기 했듯이 이러한 증상을 호소하는 다양한 질환이 있다. 크게 보면 1) 남성형 탈모 2) 여성형 탈모 3) 휴지기 탈모 4) 원형 탈모 5) 흉터성 탈모 6) 기타 희귀성 탈모로 구분 될 수 있겠다. 이 글에서는 주로 남성형·여성형 탈모 및 휴지기 탈모를 다룰 예정이다.
Ⅱ 탈모의 원인
통상 일반인들은 스트레스를 받아서 탈모가 발생한다고 얘기하지만, 탈모의 원인은 다양하며, 의학적으로는 질환을 구분하여 접근하는 것이 필요하다.
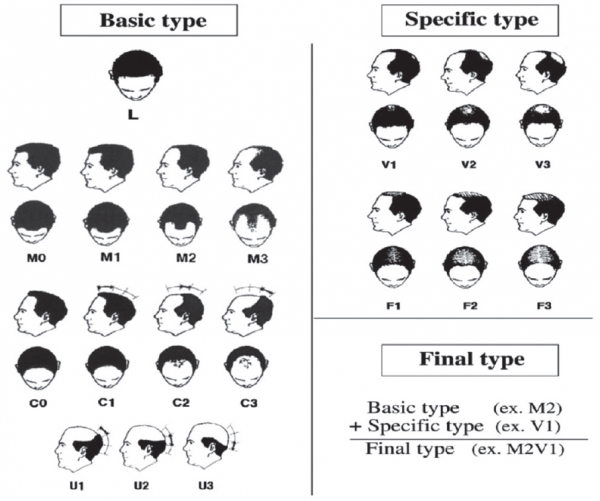
남성형 탈모(Male Pattern Baldness)와 여성형 탈모(Female Pattern Hair Loss)는 탈모가 특별한 형태를 취하며 발생하는 것으로 남성의 경우 주로 ‘M’, ‘C’, ‘U’, ‘V“ 타입으로 발생하고, 여성의 경우는 ’F’ 타입으로 발생한다(그림 1).[2] 이 두 탈모가 주로 안드로겐 호르몬인 테스토스테론(Testosterone)과 디하이드로테스토스테론(Dihydrotestosteeone)의 의해 발생하게 되므로 이러한 병태생리를 기반으로 안드로겐성 탈모(AndroGenetic Alopecia, AGA) 라고 하였으며, 최근에는 이러한 형태의 탈모를 유발하는 원인이 1) 유전, 2) 호르몬의 작용, 3) 노화, 4) 환경적 요인 등이 복합적으로 관여하여 발생하는 것으로 보고 있어, 형태에 따라 남성형 혹은 여성형 탈모로 명명하는 경향이 있다. 특별히 남성의 경우에는 유전에 의한 안드로겐 호르몬의 작용이 주된 원인으로 지목되어 안드로겐성 탈모(AGA)라 부르며, 여성의 경우는 어느 한 요인이 크게 작용하는 것이 아닌 앞서 제시한 4가지 원인 등이 좀 더 복잡하게 상호 작용하게 되므로 주로 여성형 탈모(FPHL)라고 부른다.
이러한 남성형, 여성형 탈모가 발생하는 기전은 안드로겐 호르몬이나 다양한 요인으로 인하여 모발이 점점 가늘어져 가는 일련의 과정에 의해 발생하는 것이다. 탈모라고 할 때는 모발이 어느 순간에 없어지는 것이 아니라, 모낭이 서서히 소형화 되면서 모발이 가늘어지고, 어느 순간에는 모낭과 모발이 없어지는 것이다. 이에 대해서는 남성형 탈모에서 그 기전이 아주 잘 설명되어 지는 것으로 대표적인 남성형 호르몬인 테스토스테론에서 5 알파 환원제(5 alpha reductase, 5AR)에 의하여 DHT(DHT는 안드로겐 수용체에 테스토스테론에 비하여 100배 강하게 결합하는 능력이 있다.)로 전환되어 안드로겐 수용체(Androgen receptor, AR)에 결합하고, 이 후 모낭의 소형화가 발생하는 것이다. 아직까지 DHT가 AR에 결합 후 어떻게 모낭의 소형화가 발생하는지 그 이유에 대해서는 명확하게 제시된 것은 없지만 최근 연구에 의하면 DHT가 AR에 결합 후 다양한 Paracrine mediator 들에 의하여 발생하는 것으로 제시되기도 한다.[3] (그림 2)
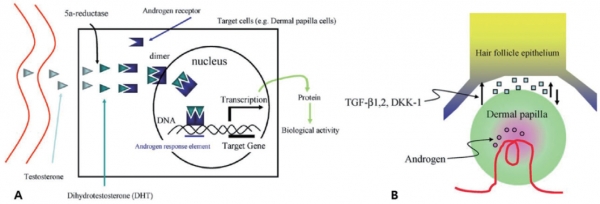
A: 안드로겐성 탈모에서 Testosterone, 5αreductase, DHT의 역할.
B: Androgen 작용에 의한 Paracrine mediator의 역할 (TGFβ, DKK-1).
환경적 요인에서는 서구화된 식생활 습관이 어느 정도 탈모에 기여하는 것으로 알려져 있다. 특히 흡연은 탈모를 유발하고, 탈모 치료의 반응을 약하게 하는 주된 원인이다.
휴지기 탈모는 급성 휴지기 탈모와 만성 휴지기 탈모로 구분이 되며, 급성 휴지기 탈모는 탈모 발생 약 3~6개월 전에 육체적, 정신적 스트레스(수술, 새로운 질병의 발병, 체중 감소, 출산, 심리적 스트레스 등)에 의하여 갑작스럽게 모발이 생장기에서 휴지기로 넘어가서 발생하는 것이다. 만성 휴지기 탈모는 원인이 미상인 경우가 아직까지 많으며, 오랜 시간 서서히 탈모가 진행되는 것으로 때로는 여성형 탈모와 구분이 쉽지 않은 경우도 있다.
Ⅲ 탈모 치료제 개발을 위한 연구 및 평가법
1) 치료제 개발을 위한 주요 타깃
탈모의 원인으로 앞서 유전과 호르몬, 노화 및 다양한 환경적 요인에 의하여 모낭이 소형화되거나 스트레스에 의하여 급격히 휴지기로 전환되어 탈모가 발생한다고 하였으므로 탈모 치료제 개발 또한 이러한 원인을 타깃으로 하여 진행된다.
가령 유전의 경우는 아직까지 탈모 관련 유전자 조작을 할 수는 없지만, 탈모를 유발할 가능성이 있는 환자를 조기에 확인하여 치료 할 수 있도록 하고자 탈모 조기 진단 유전자 알고리즘이 개발되고 있다. - 참고로 본 연구소에서도 유전자 기반 한국형 탈모 조기 진단 알고리즘을 유전체 회사와 함께 개발 중이다.- 다만 최근 유전체학의 발전에 따라 탈모 부위와 비탈모 부위에서의 Transcriptomics 분석을 통한 mRNA 전사체의 증가 패턴 등을 확인하고 이를 타깃으로 하여 발모제 치료의 개발을 하는 연구도 활발하다. 그 대표적인 예로 남성형 탈모의 새로운 치료제로 PTGDS(Prostaglandin D2 synthase)를 조절하거나 이의 타깃인 Prostaglandin D2(PGD2), GPR44 receptor를 타깃으로 하는 연구 등이다.[4]
호르몬의 경우는 주 치료 타깃이 테스토스테론과 DHT 그리고 이들의 전환에 관여하는 5 알파 환원제(5alpha reductase;5AR)를 조절하는 것과 연관이 있다. 이를 조절하는 가장 대표적인 약제가 현재 남성형 탈모에서 가장 많이 사용되고 있는 피나스테리드(Finasteride)이다. 최근에는 국소 안드로겐 수용체AR를 저해하는 치료제가 외국에서 개발 중이다.
그 외 노화나 스트레스 같은 환경적인 요인에 대해서도 다방면의 연구가 있으며, 여성에서는 특히 미네랄의 불균형–철분 부족 등-등이 제시되기도 하여 이들을 조절할 있는 항산화제나 건강 기능 식품, 그 밖의 다양한 기능성화장품들이 개발되고 있다.[5] 최근에는 이슈화된 미세먼지가 주요 연구 테마로 자리 잡고 있으며, 미세 먼지가 바로 직접적으로 탈모를 유발한다는 직접적인 증거는 없지만 두피 환경에 어떠한 영향을 미칠 것으로 생각되어 이에 대한 연구도 활발하게 진행되고 있다.
2) 세포를 통한 효능 연구
세포 연구는 주로 인체 모낭 조직에서 분리 가능한 모유두 세포(Dermal papilla cell-DP cell)와 외모근초세포(Outer root sheath cell- ORS cell)를 이용하여 연구를 진행한다. 모유두 세포는 모낭의 모근부위에 존재하는 모유두에서 일차 배양 가능한 세포로, 피부에 존재하는 중간엽 세포(Mesenchymal cells)이자 진피세포로 Matrix층에 존재하는 표피와 상호작용을 통해 모간(Hair shaft)의 성장과 모낭 주기를 조절하는 핵심 세포이다. ORS 세포는 모낭을 둘러싸고 있는 표피층으로부터 유래된 세포로, 세포 증식과 이동을 통해 모간의 두께 및 모간 증식을 조절한다. 또한 ORS는 모낭 Bulge 부분에 존재하는 줄기세포를 일부 포함하고 있는 것으로도 알려져 있다. (그림 3)
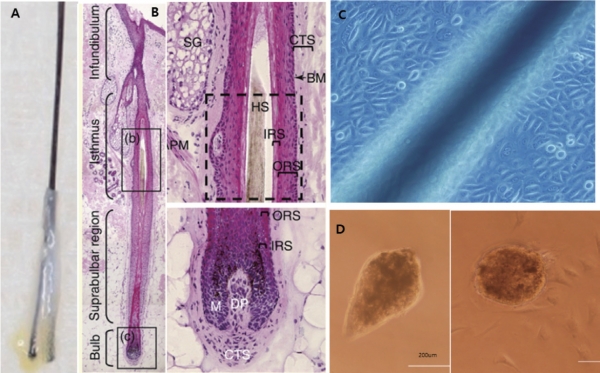
A : 실제 분리된 ex-vivo 모낭.
B : 모낭의 조직학적 구분(ORS : out root sheath, IRS : inner root shea th,M: matrix).
C : ORS 세포 배양의 실제.
D : DP(Dermal papilla) 세포 배양의 실제.
탈모 완화 치료제 개발을 위한 세포 실험에서는 가장 기본적으로 이 두 세포를 평면 배양하여 MTT assay 등을 통한 세포 독성이나 증식 및 모낭성장에 긍정적인 유전자와 단백질 발현 정도를 살펴 볼 수 있다. 조금 더 발전된 연구실에서는 조건화된 상황을 만들어서 시료와 이들 세포의 연관성을 살펴 볼 수 있다. 예를 들어 안드로겐성 탈모의 경우 안드로겐 호르몬의 작용이 중요하므로 안드로겐 수용체AR를 과 발현한 모유두 세포를 제작하여 일정 농도의 안드로겐에 노출 시킨 후 ORS 세포과 함께 공배양하여 이들의 세포의 증식, 유전자 및 단백질 발현변화를 관찰한다. 혹은 HEK 293 세포에 5-AR의 과 발현 세포를 만들고 이를 활용하여 탈모 치료제 개발 시료의 5 알파 환원 억제기능을 평가할 수도 있다.[6] 최근에는 모낭의 입체적 구조를 활용하여 모유두 세포를 원형의 3차원적 배양을 한 후 시료의 모낭형성능에 미치는 영향도 평가할 수 있겠다. 대학병원에 기반을 둔 본 연구소 같은 곳에서는 IRB의 연구 승인 하에 병원에서 얻을 수 있는 두피 조직으로부터 모유두 세포와 모낭 각질 세포를 일차 배양하여 실험에 주로 사용하게 된다.[7] 때로는 이들 세포를 저온 냉동 보관 후 사용하기도 하지만 냉동 후 해동 시 발생하는 세포 성장의 저해, 특히 ORS 세포의 경우는 이런 현상이 더욱 잘 발생하므로 실험에 주의가 필요하다. 최근에는 이러한 세포 수준에서의 스크리닝 방법을 in vivo 환경에 유사하게 모방하는 장기 칩(Organ on the chip) 개발이 한창이다(그림 4). 장기 칩은 장기를 구성하는 세포나 기관을 배양하여 in vivo상의 해당 장기의 기능, 특성, 역학적, 생리적 세포 반응을 확인할 수 있도록 유사하게 만든 시스템으로, 본 연구소에서도 의공학과, 나노 바이오 의학과와 협업하며 연구를 일부 진행하고 있다.
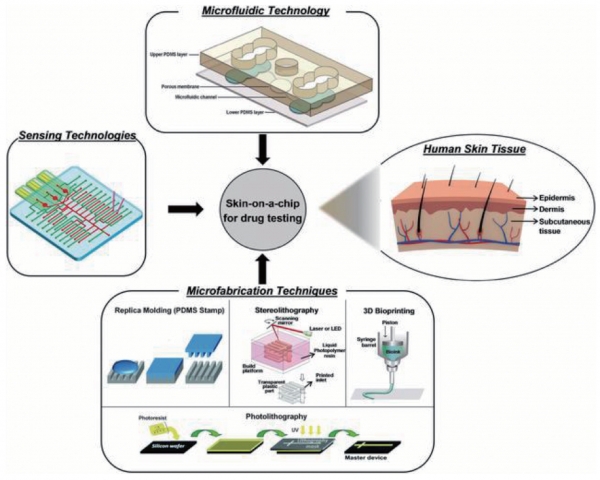
3) 모낭 기관 배양(Hair organ culture)을 통한 효능 평가
모낭은 비록 작지만, 그 자체가 신장, 간, 심장, 위처럼 하나의 기관으로 분류된다. 그러기에 우리가 신장 이식, 간 이식 등을 하듯이 탈모에서도 모발 이식이 가능하다. 이러한 모낭은 내부 고형 장기 기관과는 다르게 작고, 다수를 얻을 수 있다는 장점이 있어 직접 실험적으로 기관 배양을 통해 물질의 유효성 검토가 가능하다. 특별히, 세포 실험에서의 좋은 결과가 곧바로 임상에서의 좋을 결과를 보증하는 것은 아니기에, 임상 연구를 수행하기 전에 모낭 기관을 통한 ex-vivo 테스트를 하는 것은 세포 실험의 한계를 극복하는 대안이 될 수 있다. 다만 모낭 기관 평가를 위해서는 인체 유래의 다수의 모발이 필요하므로, 이는 병원 기반의 연구소와 협업 하지 않으면, 쉽게 수행할 수 없는 단점이 있다. 대학병원(피부과) 기반의 본 연구소에서는 자체 연구뿐 아니라, 여러 제약 혹은 화장품 회사들로부터 의뢰를 받아 개발된 시료의 모낭 기관 평가를 하고 있으며, 그 방법에 대해 잠시 소개하고자 한다.
인체 모낭은 모발이식에서 탈락된 후두부 모낭이나 외과 시술시 제거되는 두피 조직에서 시술환자의 동의를 얻어 사용할 수 있다. 모낭 그 자체를 기관배양하면 시간이 지남에 따라 (통상 7~14일 사이) 생장기에서 휴지기로 진행한다. 따라서 실험은 통상 7~14일 안에 이루어진다. 분리된 두피 조직은 Blade를 이용하여 육안으로 진피와 피하지방층으로부터 모낭을 단일 가닥으로 분리한 후, 입체 현미경상으로 모유두와 진피층의 손상이 없는 성장기 모낭만을 사용하여 실험에 사용한다. 분리한 모낭은 각 군별로 약 5~6개의 모낭을 액침배양법으로 모낭배양 배지 또는 시료를 첨가하여 배양하고, 모낭 길이의 성장 또는 성장기Anagen의 유지 효과를 현미경상에서 확인할 수 있다 (그림 5). 나아가 이렇게 배양한 모낭을 동결 절편을 제작 후 모낭 조직 슬라이드상에서 모낭성장과 관계된 다양한 단백질들의 염색을 통해 모낭기관상에서 타깃 단백질이 발현되는 위치를 분석할 수 있다.[8]

A : 모낭 기관 평가의 진행과 평가.
B : 배양 날짜에 따른 모낭의 길이 성장의 실제.
4) 실험동물을 활용한 효능 평가
2015년 식약처의 탈모 방지제 효력 평가 시험법을 보면 동물 실험을 통하여서도 탈모 방지제의 평가가 가능하다고 되어 있으나 화장품 원료의 동물 실험이 금지되어 있다. 2018년 개정된 탈모 증상 완화에 도움을 주는 화장품의 인체적용시험 가이드라인에서도 동물 실험은 제외되어 있으므로 이 글에서도 생략한다. 다만 동물의 기관을 빼어 내어 ex-vivo 테스트를 하는 것은 가능할 것으로 생각되어 이에 대하여 소개하고자 한다. 이를 위해서는 수컷 Sprague Dawley 흰쥐의 전립선을 활용한다. 적출된 전립에서 만들어진 Male SD rat의 전립선 균질화 상등액을 활용하여 5-AR 활성 억제작용을 측정할 수 있다. 이때는 5-AR의 활성도를 직접 측정하는 것은 아니며, 테스토스테론에서 DHT로 전환되는 정도를 평가하여 5- AR의 억제 능력을 평가하는 것이다(그림 6).
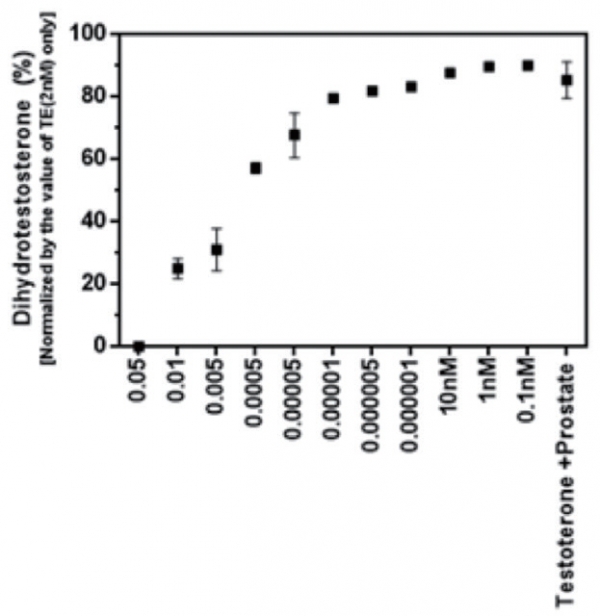
‘A’ 시료의 농도가 증가함에 따라 5 알파 환원제가 억제되어 DHT 의 농도가 감소하는 것이 보인다.
5) 탈모 증상 완화에 도움을 주는 화장품의 인체 적용 평가
양모제의 임상 평가에 대해서는 식약처의 임상 효능 평가 가이드가 제정되어 이 가이드를 따라서 연구를 수행하게 된다. 역사적으로는 2009년 12월에 처음으로 양모제 효력평가시험법 가이드라인이 제정 된 이후 2015년에 탈모 방지제 효력 평가 시험법 가이드라인으로 개정되었다. 이후 최근 2018년 7월에 탈모 증상 완화에 도움을 주는 화장품의 인체적용시험 가이드라인으로 재개정 되었다.
최신 개정 가이드라인에서는 식약처의 기능성화장품 효능 인정을 받기 위하여서는 통계적으로 유효한 값을 확인하기 위하여, 대조군과 치료군 각각에서 최소 유효 피험자를 20명 이상 하도록 규정하고 있다. 따라서 약 20%의 탈락률을 고려하면 안전하게 연구를 진행하기 위해서는 대조군과 치료군에서 각각 25명씩 전체적으로 50명의 피험자를 모집한다. 연구 기간은 모발의 주기를 고려하여, 화장품의 효능에 대한 평가는 최소 24주 이상 하도록 하였다. 연구 방법은 무작위 배정, 이중맹검, 대조군 비교 인체적용시험을 원칙으로 한다. 1차 유효성 평가 변수는 포토트리코그램(phototrichogram-PTG)에 의한 단위 면적1cm2 당 총 모발 수의 변화를, 2차 유효성 평가 변수는 ① 사진촬영에 의한 전문가 육안 평가, ② 피험자 설문 평가 이다. 연구 결과 평가 기준은 동일 위치에서 측정한 1cm2 원내에 있는 모발수가 대조군에 비해 제품 적용 후 최소 24주 이상에서 통계학적 유의한 효과를 보여야 하며, 2차 유효성 평가 변수에서 이를 뒷받침할 수 있는 효과를 확인하여야 한다.
탈모 임상 연구 수행에서 가장 중요하고도 주의해야 할 점은 PTG의 촬영이다. 두피 문신을 기준으로 방문시 이전 사진과 동일한 부위를 동일하게 촬영하는 것이 가장 중요하다. 가이드라인에서 ‘매번 점 문신 또는 일정좌표를 중심으로 하여 포토트리코그램을 시행한다.’ 라고 되어 있지만 문신이 있다 하더라도 첫 시작의 사진과 동일하게 촬영하는 것은 쉽지 않으며, 숙련이 필요하다. 특히 단위 면적1cm2의 기준을 정하는 정사각형 혹은 원형의 경계 부위에 모발이 있는 경우는 그 평가에서 0 주차 사진과 16주차, 24주차 평가에서 그 포함 여부를 일관성 있게 하여야 한다.
전문가 육안 평가 역시 동일한 조건, 구도 및 위치에서 45도 (앞머리선), 90도(정수리) 두 부위를 평가 촬영하는 것이 필요하며, 이를 돕기 위하여 다양한 장비가 있으므로, 이를 활용하는 것도 좋을 것 같다. (그림 7)
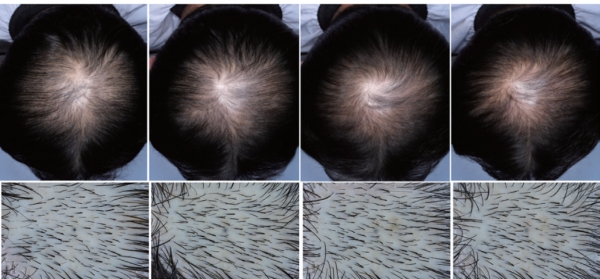
결론
탈모는 외모와 직접적으로 연관되고, 삶의 질과도 연결되어, 피부과 질환 중에서도 대중적 관심이 높은 질환이다. 따라서 탈모 진행의 완화를 위한 의약품, 의료기기 및 기능성 화장품에 대한 연구와 개발은 지속적으로 활성화 될 것으로 생각된다. 이에 우리는 이 글을 통해 탈모 완화 치료제 개발을 위하여 탈모의 발생 기전에 대해 살펴 보았으며, 또한 탈모제의 개발과 평가를 위한 기초 실험과 임상 연구가 어떻게 진행되고 있는지 다양하게 살펴보았다. 이 글이 대한민국 경제의 한 축인 뷰티 산업의 현장에서 기능성화장품의 개발에 열정을 쏟고 있는 많은 연구 종사자분들에게 조금이나마 도움이 되길 바란다.
REFERENCES
1. 피부과학 제 6판 대한의학 p550-555
2. J Am Acad Dermatol. 2007l;57(1):37-46.
3. Journal of Dermatological Science 2011;61:1–6
4. Sci Transl Med. 2012 March 21; 4(126): 126ra34
5. Journal of Korean Medical Science 2013;28:934-938
6. Journal of Steroid Biochemistry & Molecular Biology 2007;107:245-252
7. Experimental Dermatology 2002;111:381-385
8. Experimental Dermatology 2015;24:903-911